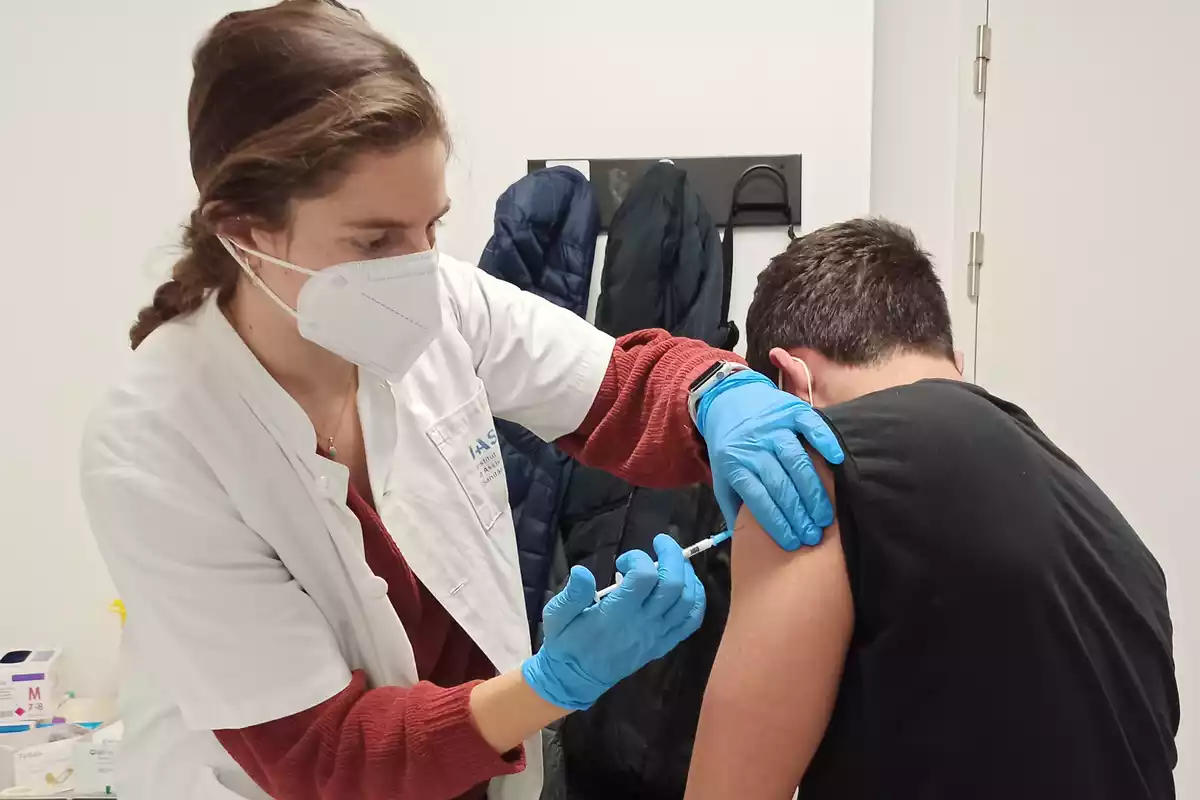
La vacuna de la farmacèutica catalana Hipra fa un temps que ha estat autoritzada a utilitzar-se per prevenir la covid-19. El vaccí cada cop va superant fases i ara n'ha arribat a una de nova.
L'Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) ha autoritzat un segon assaig clínic fase IIb de la vacuna. Un procés que té com a objectiu determinar i comparar els canvis en la immunogenicitat contra la variant òmicron en els voluntaris que han rebut dues dosis de la vacuna d'AstraZeneca i la d'Hipra com a dosi de reforç.
Fins ara, les persones que se'ls havia administrat el vaccí d'AstraZeneca, rebien la dosi de reforç amb la de Pfizer.
En l'assaig que s'havia fet abans que aquest, autoritzat el 15 de novembre, l'estudi es feia amb voluntaris que havien rebut els vaccins de Pfizer. L'assaig actual es durà a terme en cinc centres hospitalaris de l'estat espanyol i comptarà amb la participació de 300 voluntaris.
El nou assaig amb Hipra
Aquest nou assagi serà aleatori, controlat i doble cec. Això vol dir que s'administra la vacuna d'Hipra o una autoritzada emmascarada, de manera que ni el pacient ni l'equip investigador pugui identificar quina es posa.
Els centres hospitalaris començaran tan aviat com puguin a seleccionar els voluntaris que compleixin amb els requisits necessaris. Aquests no hauran d'haver passat la covid-19, hauran d'haver rebut dues dosis de la vacuna d'AstraZeneca com a mínim 91 dies si només de 365 dies després de l'administració de la segona dosi. Rebran una única dosi de reforç.
Per autoritzar l'estudi s'ha tingut en compte que en els tres assaigs ja autoritzats sobre aquesta vacuna no s'han detectat problemes de seguretat i només s'han trobat les reaccions esperables en l'administració de vaccins.
L'assaig en fase II, autoritzat l'1 de febrer, busca avaluar la seguretat i tolerabilitat de la vacuna com a dosis de reforç de qualsevol de les vacunes autoritzades fins ara en una major mostra de voluntaris que els citats aquest cop.
La vacuna d'Hipra contra la covid es basa en dues proteïnes, una corresponent a la variant alfa i una segona a la beta. Totes dues s'uneixen formant una estructura única anomenada dímer i que està acompanyada d'un adjuvant que incrementa la resposta immunològica.
Aquesta combinació és capaç de generar una resposta contra una de les proteïnes del SARS-CoV-2, la S. Aquesta plataforma, tot i que expressa proteïnes de dues variants diferents, és la mateixa que s'ha fet servir per a la vacuna Novavax, que està en procés d'avaluació per part de l'Agència Europea del Medicament (EMA).